检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox

邮 箱:
所属实验室:宋艳实验室
我们课题组致力于探索脑发育中细胞命运决定和细胞命运记忆传承的分子调控机理及相关神经发育疾病的发生与防治。
1. 脑发育中的细胞命运记忆 – 有丝分裂书签
咬定青山 - 有丝分裂书签维持神经干细胞命运记忆
细胞的命运和身份主要由其独特的基因调控网络决定和维持。细胞命运决定或维持过程出现错误均可能导致疾病发生。然而,有丝分裂却给细胞命运或身份的跨代继承带来了巨大挑战。细胞在进入有丝分裂后,染色质高度凝集成染色体,绝大多数构成基因调控网络的元件从染色体上剥离或降解,转录活动几乎完全停滞。随着其独特基因调控网络在有丝分裂期的“分崩离析”,细胞好似进入短暂失忆状态。那么,细胞在退出有丝分裂进入分裂间期时,是如何精确、及时地重建其独特的基因调控网络的呢?关乎细胞命运或身份的“记忆”在有丝分裂期如何被精确储存,在分裂间期又如何被及时唤醒呢?
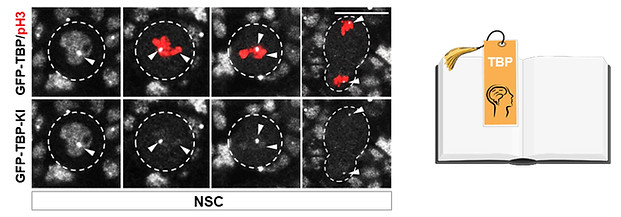
我们的最新研究发现在神经发育过程中,转录因子TBP通过招募染色质重塑因子EP400增加局部染色质可及性,作为有丝分裂书签保留在神经干细胞染色体上,进而维持神经干细胞的命运记忆。这项研究发现书签蛋白的有丝分裂保留促进神经干细胞自我复制和增殖,首次揭示了有丝分裂书签对神经发育的重要生理学意义,并阐明了书签蛋白通过调控局部染色质可及性实现染色体保留的新机制。值得一提的是,该研究建立了一个全新的技术方案,实现对发育脑中书签蛋白在染色体上的保留位点的精确鉴定。这一新方法将助力有丝分裂书签在其它物种和其它组织器官中的发现及其生理学功能和机制研究的开展。这一研究成果于2024年12月发表于国际知名学术期刊 Molecular Cell。
原文链接: http://doi.org/10.1016/j.molcel.2024.11.019
简介: https://mp.weixin.qq.com/s/VftxDuaIhvym1ybTzn7Hlg
前世今生 - 植入染色体的转录因子凝聚体驱使神经元终末分化
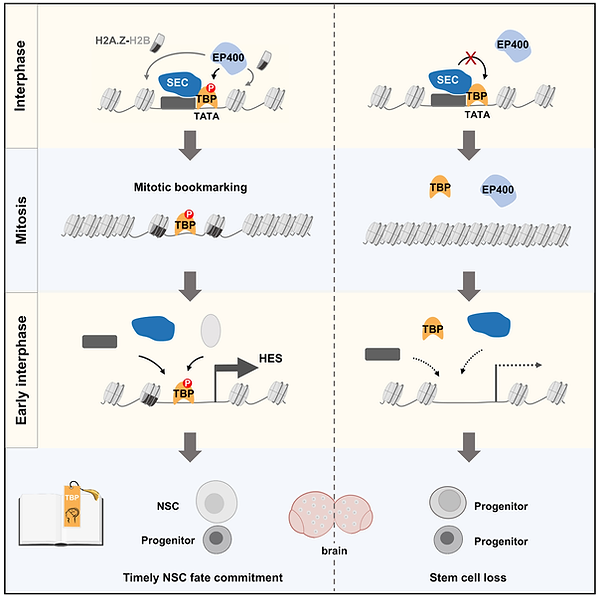
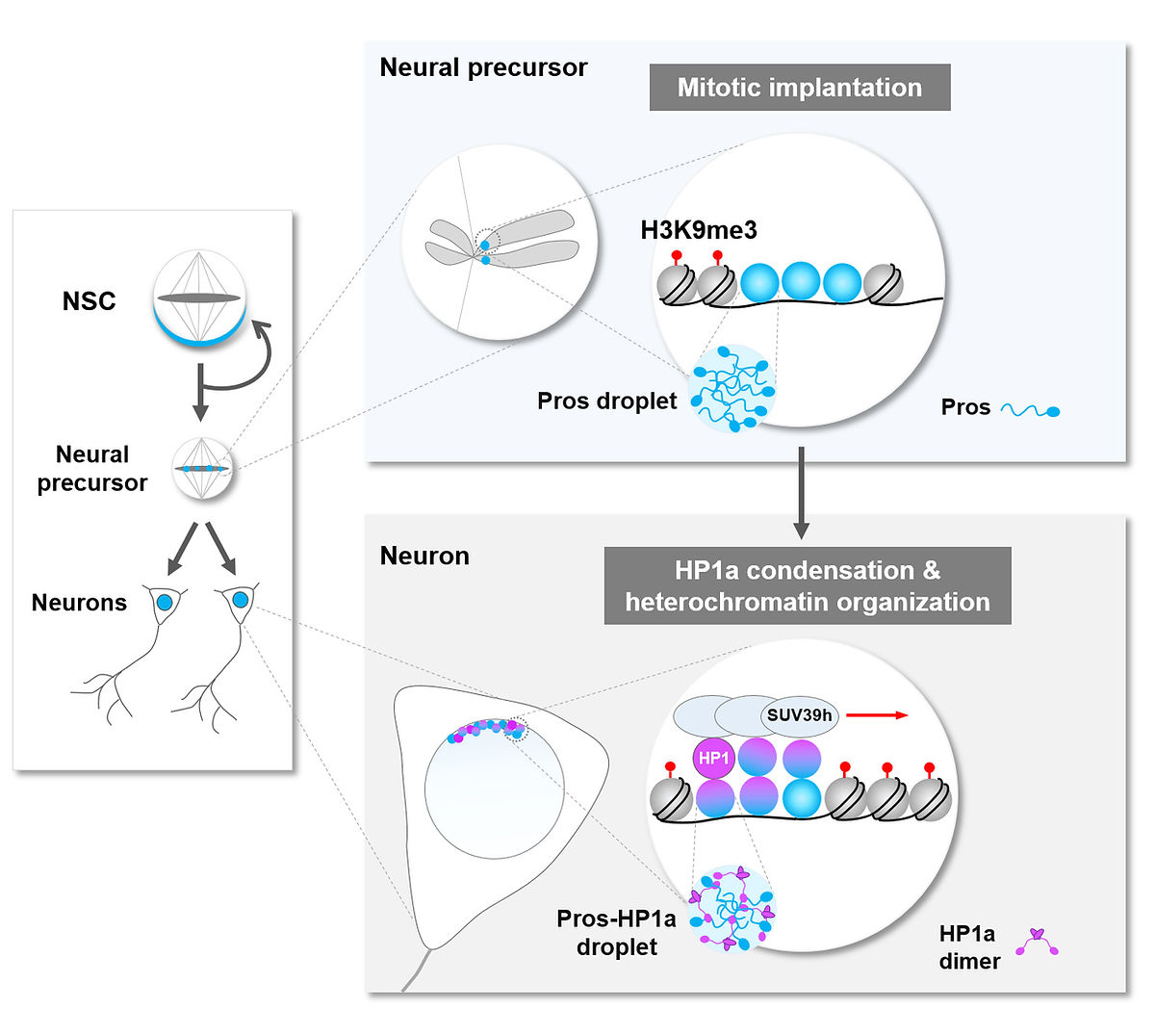
异染色质区域在细胞终末分化过程中如何凝聚和扩展一直以来都是悬而未决的重要科学问题。我们近期的研究发现一个在进化上高度保守的转录因子Prospero通过液-液相分离得以植入神经前体细胞有丝分裂染色体的异染色质区域,进而通过促进异染色质区的凝聚和扩展形成转录抑制环境,永久沉默自我复制相关基因的表达,通过选择性删除相关细胞记忆,驱使新生神经元彻底忘记其进行自我复制的“前世”,在“今生”当好终末分化的神经细胞。这项研究出乎意料的结果揭示了转录因子通过其生物物理特性的变化引起异染色质结构重塑,进而驱动细胞终末分化的新机制。同时,这项研究首次建立了转录因子的液-液相变与生理条件下一系列重要生物学事件之间的因果关系,为相分离在动物发育过程中的重要生理学意义提控了强有力的证据。作为亮点推荐文章(featured article) , 这一研究成果于2020年2月发表于国际知名学术期刊 Developmental Cell。杂志同期还配发了评述文章和亮点推荐。
原文链接:https://www.cell.com/developmental-cell/pdf/S1534-5807(19)30990-6.pdf
简介:http://bio.pku.edu.cn/homes/Index/news_cont/22/14899.html
好签成双 -“双书签”机制调控脑发育中细胞命运记忆的差异传承
在神经干细胞进行不对称分裂生成两个命运迥然不同的子代细胞的过程中,细胞记忆是如何被不对称地传递和继承的呢?换句话说,细胞命运记忆是如何在一个子代细胞中被精确保存而在另一个子代细胞中被及时删除的呢?借助实验室新近开发的鉴定发育脑中有丝分裂书签基因组结合位点的BISMIB组学技术 (Shen et al., STAR Protocols, 2025) 并结合精细的分子遗传学、细胞生物学、液-液相分离、生物化学和其它多组学技术,我们的最新研究揭示了一种全新的“拮抗性双重有丝分裂书签标记与选择性分子竞争相结合”的机制,实现细胞命运记忆在姐妹子细胞中的差异性继承。这项研究首次发现和提出有丝分裂书签可以“组合使用”。有丝分裂书签通过时空动态排列组合,大大拓展了其可能标记的基因位点和细胞类型,使得复杂多样的神经细胞命运记忆的精确储存和跨代继承成为可能,进而为极度精妙复杂的大脑构建过程保驾护航。这一研究成果于2025年8月发表于国际知名学术期刊 Nature Communications。
原文链接: https://www.nature.com/articles/s41467-025-62974-6
简介: https://www.bio.pku.edu.cn/homes/Index/news_cont/22/17902.html
是我非我 – “有丝分裂书签”机制定义和维持海马体齿状回神经谱系身份
我们最新的工作发现了第一枚哺乳动物发育脑中真正意义上的有丝分裂书签 Prox1, 成功鉴定了它在海马体齿状回神经干细胞染色体上标记的关键基因位点,确认了其作为有丝分裂书签的重要生理学意义及分子调控机理-通过删除“非我”的神经谱系记忆来“定义”正确的谱系身份。
原文链接: https://www.biorxiv.org/cgi/content/short/2026.02.25.707603v1
2. 脑发育中的细胞命运锁定与疾病发生
盘古开天 – “信号放大器”机制驱使神经干细胞命运及时锁定
干细胞自我更新与分化间精妙平衡的打破会引起组织稳态失衡,进而导致发育缺陷和癌症发生。我们的研究发现由神经干细胞不对称分裂最初建立的子细胞间的微小差异需要经过一个快速放大的阶段才能被最终锁定为两个截然不同的子细胞命运,并揭示超级延伸复合物 SEC 通过“信号放大器”机制,驱动这一放大过程快速、精确、稳健地完成。这项研究所揭示的细胞内放大器机制代表了一种细胞自主调控不对称分裂后子细胞命运锁定过程精确性与稳健性的普适规律。此外,该研究也为超级延伸复合体的过度激活与多种人类癌症的相关性提供了全新的理论解释。该研究发现于2017年3月作为封面文章 (cover article) 发表于发育生物学领域顶级期刊Developmental Cell。杂志同期还配发了评述文章和亮点推荐。
原文链接:https://www.cell.com/developmental-cell/pdf/S1534-5807(17)30118-1.pdf
简介:http://bio.pku.edu.cn/homes/Index/news_cont/22/4151.html

拆弹为安 - 神经祖细胞命运及时锁定与脑肿瘤发生
我们的研究发现 Retromer 复合体作为“拆弹部队”将神经祖细胞内可能被“引爆”的 Notch 受体及时“拆除”并运离,从而确保神经祖细胞命运的及时锁定。该研究揭示的由 Retromer 复合体介导的保护机制可能代表了一种普适规律:通过该机制,潜在有害或有毒的蛋白受体可以被及时清除,从而避免不良的后果。该研究也为解析 Retromer 复合体失活与多种人类癌症相关性的分子机制提供了重要线索。该研究发现于2018年9月发表于eLife 杂志,获得了同期杂志的特别新闻推送。
原文链接:https://elifesciences.org/articles/38181
简介:http://bio.pku.edu.cn/homes/Index/news_cont/22/4039.html
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox