检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
2026年5月6日,北京大学生命科学学院、北大-清华生命科学联合中心、北京大学成都前沿交叉生物技术研究院胡家志课题组在Genome Research杂志上发表了题为“Restoring the potency of a neutralizing antibody via guided hypermutation with hyper-antibody editor HAE1”的研究论文。该研究报道了用于抗体体外进化的高频抗体编辑器HAE1(Hyper-antibody editor 1),并搭建了基于哺乳动物细胞的抗体双表达系统,成功实现SARS-CoV-2逃逸抗体的亲和力进化,为抗体性能优化提供了高效技术路径。

体细胞高频突变(somatic hypermutation, SHM)是指B细胞受到抗原刺激后,由嘧啶脱氨酶(activation-induced cytidine deaminase, AID)在抗体基因上引入高频碱基变异的过程,该过程驱动了体内的抗体亲和力成熟。因此,抗体进化过程通常借鉴该过程。然而,当前主流抗体进化方法仍存在明显局限:传统噬菌体或酵母展示系统仅能表达抗体片段,难以保证全长抗体的正确糖基化修饰及功能;哺乳动物细胞展示技术结合AID过表达可模拟体内SHM,但突变效率有限,制约进化效率;结合基因编辑工具的引导超突变(guided hypermutation, GHM)工具,通过将高活性AID突变体与dCas9融合提升了进化效率,但与自然SHM过程相比,其突变种类较局限。
针对上述不足,胡家志课题组结合基因编辑与抗体进化,利用无PAM限制的Cas9突变体SpRY结合胞嘧啶脱氨酶和腺嘌呤脱氨酶,开发了高频抗体编辑器HAE1(图1A),实现了对抗体可变区任一碱基的靶向突变,拓宽了抗体进化的路径;同时,为了优化哺乳动物细胞中的抗体进化与验证流程,作者开发了一种由内含子介导的双表达系统,使其能同时表达跨膜和分泌两种类型抗体。其中,跨膜型抗体可实现突变细胞筛选分离,而分泌型抗体则便于进行抗体亲和力变化的快速验证(图1B)。
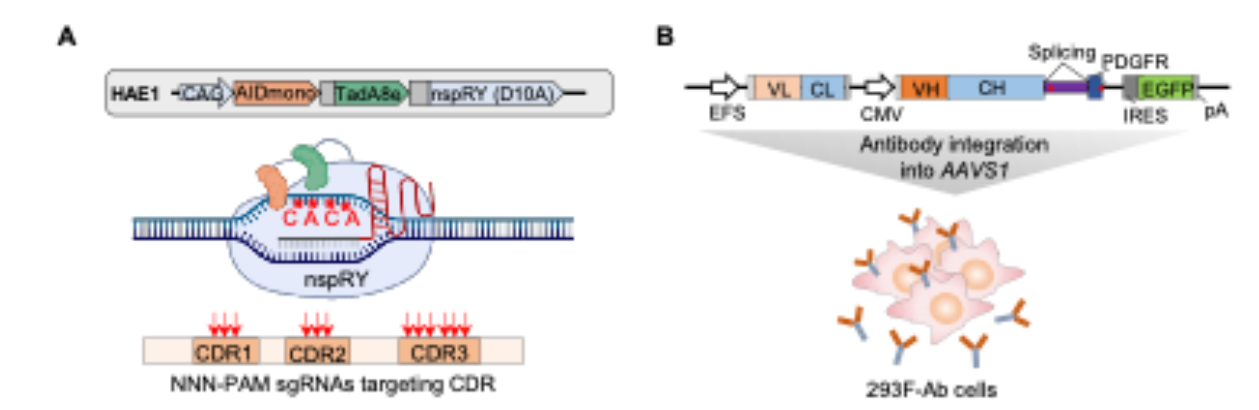
图1. HAE1组成和抗体双表达系统。A:HAE1结构示意图,NNN-PAM可以实现抗体可变区CDR的任意靶向;B:内含子通过可变剪接实现抗体跨膜和分泌型双表达。
为了验证HAE1的进化能力,研究者以SARS-CoV-2抗体CV07-209为模型(CV07-209可高效识别Delta,但无法识别Omicron),通过两轮进化结合双表达体系的高通量检测,快速筛选出两株候选抗体(图2A)。这两株抗体(P6和P42)在保持对Delta突变株识别能力的同时,显著恢复了对Omicron突变株BA.1的结合活性,并展现出高效的中和能力。而后续回复突变的实验结果则证实了Y33C(TAC > TGC)和S53I (AGT > ATC)这两位由TadA编辑引起的氨基酸突变对该抗体识别BA.1的必要性,揭示了HAE1双脱氨酶协同作用在抗体定向进化中的重要意义(图2B-C)。
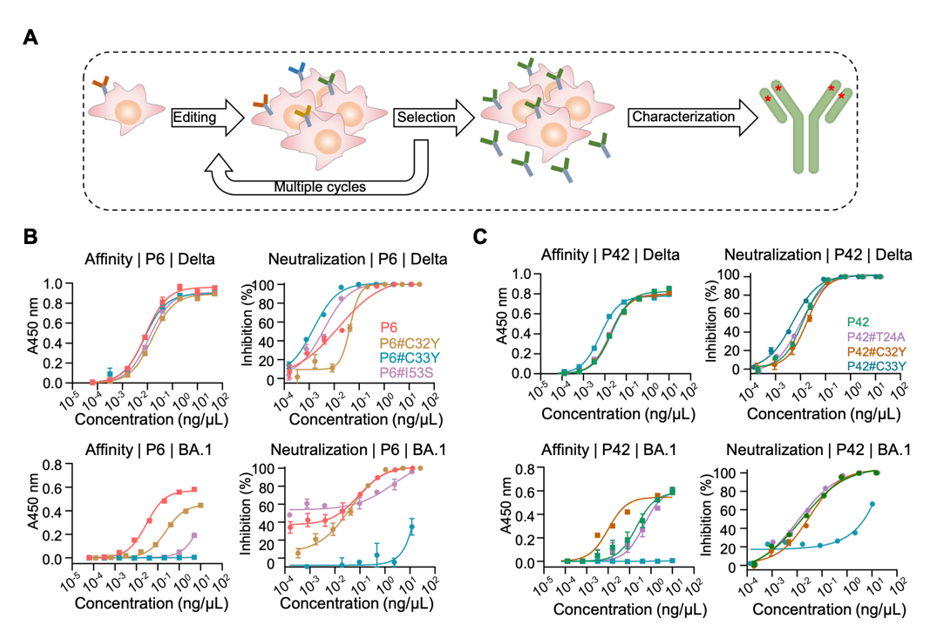
图2. 利用HAE1进化CV07-209。A:进化流程示意图,每一轮进化包含突变和筛选两个过程,总共两轮。B-C:P6(B)和P42(C)核心氨基酸回复突变检测抗体亲和力和中和能力。
最后,研究者还对比了AI模型预测的抗体亲和力成熟突变与HAE1进化抗体的差异,显示了在AI技术快速发展的时代背景下,高效抗体进化工具仍然具有重要应用价值以及为AI提供高质量训练数据的价值(图3)。
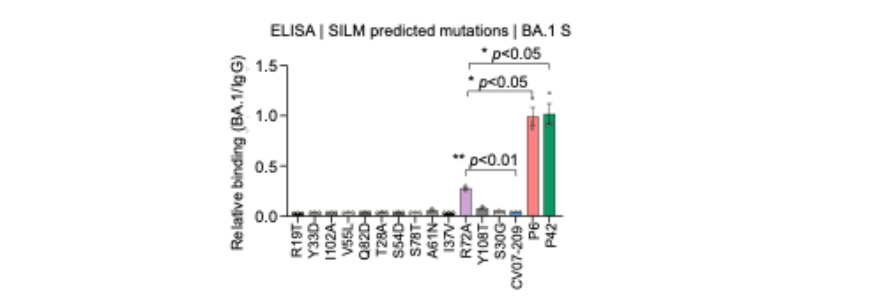
图3. SILM模型预测的抗体突变对CV07-209抗体亲和力的影响。SILM模型预测的突变中只有R72A可以初步提升原始抗体识别BA.1 S蛋白的能力。
综上所述,HAE1作为一种新型GHM工具,结合无PAM限制的SpRY和双脱氨酶系统,实现了抗体进化过程中的灵活靶向和广泛突变,犹如抗体的“点石成金笔”。虽然SpRY存在的脱靶风险限制了其在传统精准基因编辑中的应用,但其灵活性使其可以靶向抗体的任何残基,在抗体进化中具有明显优势。HAE1广谱、高效的编辑特性加速了抗体进化流程,拓宽了基因编辑工具的应用场景,也为其他蛋白质工程化领域提供了重要的技术支撑,具有广阔的应用前景。
本文通讯作者为北京大学生命科学学院、北大-清华生命科学联合中心、北京大学成都前沿交叉生物技术研究院的胡家志教授。第一作者为胡家志课题组的王渝鸿和郭岳峰博士。课题组的卢秋宇、刘心怡、陈佳艺、皮睿琦、徐浩棋、元绍鹏、杨子霆,北京大学成都前沿交叉生物技术研究院的卢如森、甘婷婷博士和中国科学院分子细胞科学卓越创新中心孟飞龙教授也为该课题的顺利完成做出了重要贡献。本项研究工作得到了国家自然科学基金、科技部重点研发计划、农业农村部、四川省自然科学基金等项目的资助与支持。
原文链接:https://doi.org/10.1101/gr.281396.125
胡家志实验室网址:https://hulab.pku.edu.cn/